

2026年2月27日,海军军医大学上海长征医院殷浩团队联合中国科学院分子细胞科学卓越创新中心(生物化学与细胞生物学研究所)程新研究组在国际顶级期刊Lancet Diabetes & Endocrinology(在191种内分泌与代谢学期刊中排名第一)发表了最新研究成果:“Autologous and allogeneic stem cell-derived islet therapy in three recipients with type 1 diabetes and complete loss of endogenous pancreatic β-cell function pretransplant”。

论文:https://www.thelancet.com/journals/landia/article/PIIS2213-8587(25)00423-1/fulltext
该项研究首先利用患者自体/健康人供体的PBMC重编程为iPSC,进而建立具有内胚层分化特异性的内胚层干细胞(Endoderm stem cell, EnSC),并以EnSC为种子细胞在体外制备自体/异体再生胰岛组织(E-islet),经皮肝门静脉穿刺移植治疗三例严重1型糖尿病(T1D)患者,并实现了胰岛功能重建与血糖自主调控。该研究提示:即使采用自体来源的再生胰岛治疗T1D,仍需长期使用“Edmonton Protocol”的标准免疫抑制方案,以克服自身免疫的再次攻击。
这是世界范围内首次报道的、分别利用干细胞来源的自体/异体再生胰岛移植治疗T1D的探索性临床研究。这项研究不仅延续了该团队此前在治愈2型糖尿病(T2D)领域的重大成果,更在“治愈1型糖尿病”领域迈出了突破性的一步,标志着中国科研团队在干细胞再生医学与糖尿病治疗前沿领域的持续引领与国际贡献。
01
采用自体或异体内胚层干细胞来源的再生胰岛(E-islet)
脆性1型糖尿病(约占T1D患者总数的5%)患者即使在接受规范治疗并严格控制饮食的情况下,仍表现为血糖控制极不稳定,严重低血糖事件频发。这类患者不仅面临高血糖所引发的多种慢性并发症风险,还可能因严重低血糖导致神经系统不可逆损伤,甚至危及生命。针对这一临床难题,近年来国际范围内已开展多项利用干细胞来源再生胰岛移植治疗1型及2型糖尿病的临床研究,初步证实了再生胰岛在人体内重建生理性血糖调控功能的安全性与有效性。
此次研究有三例严重1型糖尿病患者案例,他们分别采用自体或异体内胚层干细胞来源的再生胰岛(E-islet),并在不同免疫抑制策略下评估疗效与安全性,取得了鼓舞人心的临床结果。
值得说明的是,该三例1型糖尿病患者所用的再生胰岛(E-islet),由智新浩正(上海)医药科技有限公司基于中国科学院分子细胞科学卓越创新中心程新团队研发的“新型人内胚层干细胞(EnSC)及其胰向分化技术”制备而成(智新浩正获该技术的独占实施许可)。该技术通过精准模拟胰岛体内发育过程,在体外高效规模化制备获得E-islet。所得E-islet具备与健康胰岛一致的结构和功能,能够实时感知血糖变化,精准分泌胰岛素、胰高血糖素、生长抑素等多种内分泌激素,从而有效维持血糖稳态。
02
具体案例及成效
案例一:
自体E-islet移植治疗1型糖尿病伴低血糖频发
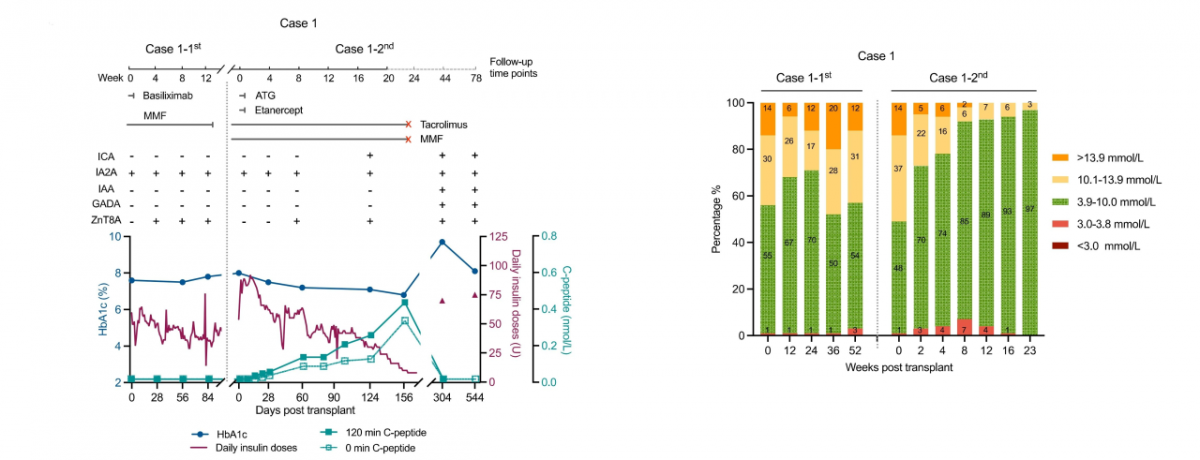
图1 案例1临床结果
患者为30岁女性,1型糖尿病病程18年,长期血糖控 制不佳,严重低血糖事件频繁发生。
首次移植(2022年4月7日):采用自体E-islet移植联合低剂量免疫抑制方案(单剂量IL-2抑制剂巴利昔单抗短期诱导,联合霉酚酸酯长期维持)。术后未见胰岛功能改善,提示该免疫抑制方案未能有效控制自身免疫攻击。
第二次移植(2023年5月12日):采用自体E-islet移植联合标准免疫抑制方案(Edmonton方案)。术后胰岛功能显著恢复:C肽水平于术后第24周恢复至正常范围;血糖控制明显改善(糖化血红蛋白从术前8.0%降至6.8%,目标范围内时间从术前48%提升至97%);每日胰岛素注射剂量从54单位减少至8单位。
随访与转归:患者于术后6个月因双相情感障碍复发,自行停用所有免疫抑制剂。停药后,五项胰岛自身抗体全部转为阳性,提示自身免疫攻击重建;胰岛β细胞功能在停药后5个月内完全丧失。
该案例关键提示:即使使用自体来源的再生胰岛治疗1型糖尿病,若缺乏足够的免疫抑制保护,仍无法避免自身免疫攻击导致的胰岛功能丧失。Edmonton方案所代表的完整免疫抑制治疗对于克服T1D患者自身免疫问题、实现胰岛功能重建至关重要。
案例二:
异体E-islet移植治疗爆发性1型糖尿病伴低血糖频发
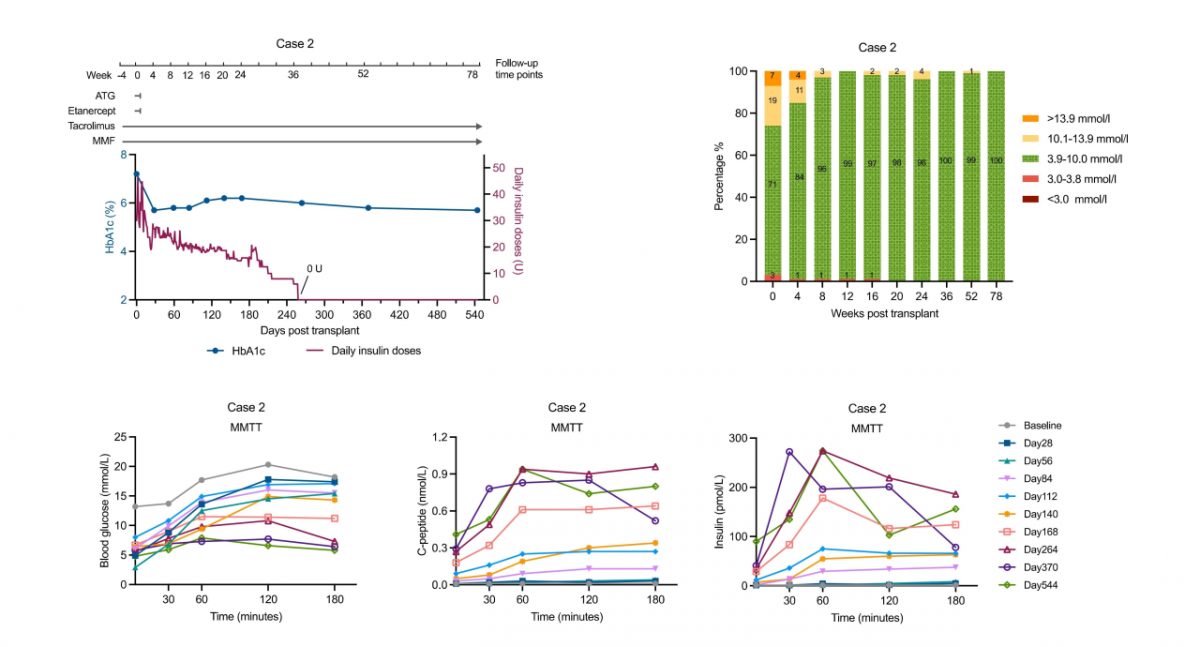
图2 案例2临床结果
患者为45岁男性,2019年确诊爆发性1型糖尿病,病程中血糖控制长期欠佳,严重低血糖事件频发。
移植方案:于2023年12月30日接受健康供体来源的异体E-islet移植,并联合标准Edmonton免疫抑制方案。
临床疗效:移植后胰岛功能逐步恢复,血糖控制显著改善:糖化血红蛋白(HbA1c)从术前7.2%降至5.7%;目标范围内时间(TIR)从术前71%提升至100%。
患者于术后第36周实现完全脱离外源胰岛素,截至数据统计时,已维持血糖平稳超过26个月。
该案例关键提示:该案例为“在标准Edmonton免疫抑制方案下,异体E-islet 移植可实现1型糖尿病患者外源胰岛素长期脱离”提供了有力的临床证据。
案例三:
异体E-islet移植治疗青少年脆性1型糖尿病
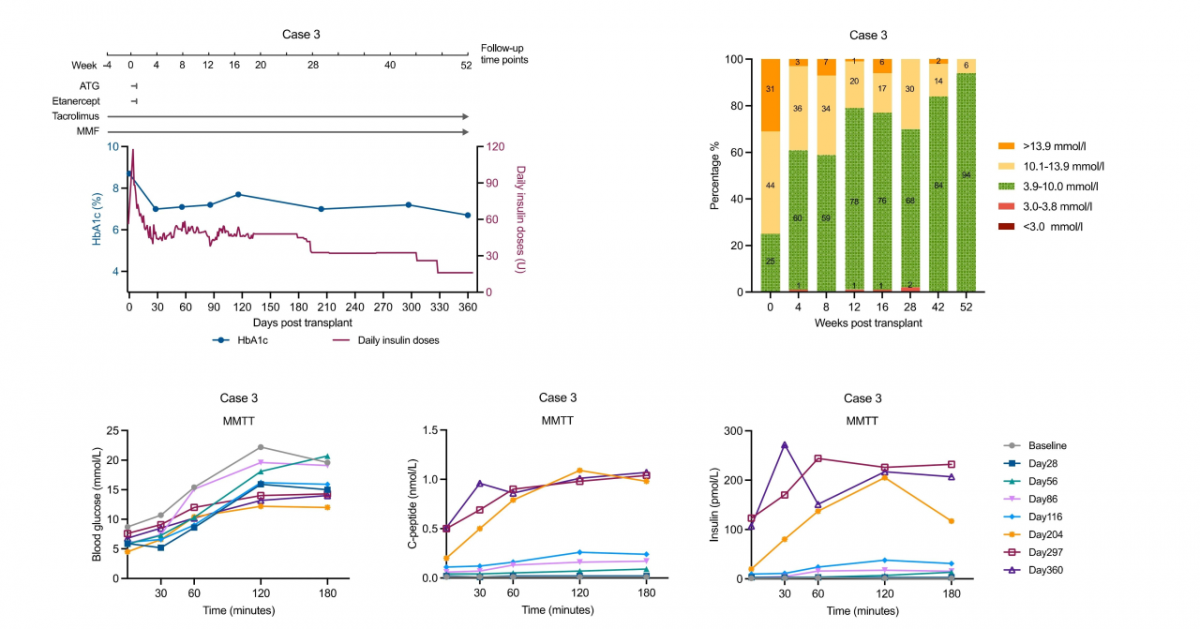
图3 案例3临床结果
患者为15岁女性,脆性1型糖尿病病程5年,长期血糖控制极差,频繁发生酮症酸中毒及严重低血糖事件。
移植方案:于2024年9月2日接受健康供体来源的异体E-islet移植,并联合标准Edmonton免疫抑制方案。
临床疗效观察:移植后胰岛功能逐步恢复,血糖稳定性显著改善:糖化血红蛋白(HbA1c)从术前8.7%降至6.7%;目标范围内时间(TIR)从术前25%提升至94%。受长期外源胰岛素使用史及青春期生理性胰岛素抵抗等因素影响,患者目前尚未实现完全脱离外源胰岛素,但严重低血糖事件已完全消失,整体生活质量显著提升。
该案例关键提示:该案例初步证实了该疗法在青少年1型糖尿病患者群体中的临床安全性与有效性,为后续在青春后期人群中开展更大规模研究提供了重要参考。
来源:智新浩正